-

- 메일앱이 동작하지 않는 경우
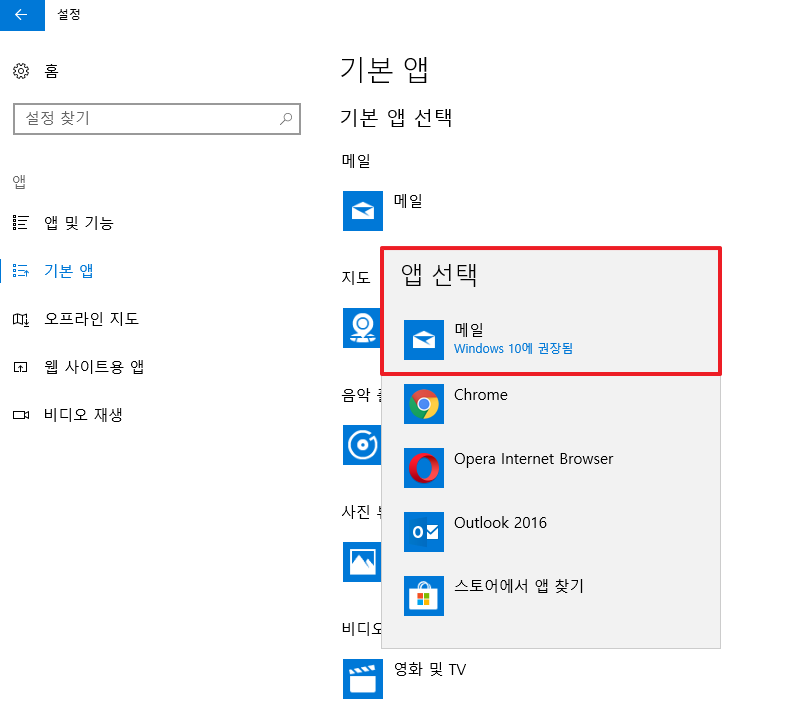
- Window 설정 > 앱 > 기본앱 > 메일에서 메일앱으로 변경
- [항만 > 스마트항만연구실]2018-04-26 10:07:36/ 조회수 2705
-
의약품 공급망이 직면한 주요과제
- 평가덧글
- 인쇄보내기
- 1) 가시성(Visibility)
공급망에 대한 가시성 부족은 제약업계가 당면한 문제이다. 의약품부족 문제, 많은 환자, 규제기관, 소매업체들이 의약품이 어디서 어떻게 제조되어 왔는지를 알지 못한다는 것이다.
운송 중 열악한 온도 관리로 인한 주요한 성분의 약병이 손실되고 회사가 그것을 증명할 수 없다면 3자 물류업체는 이러한 우려를 해결하는 것 이외에 선택의 여지가 없다. 한편 제조과정에서 의약품이 오염되었다면 공급업자가 문제를 해결하라고 요청받을 수 있습니다.
2) 의약품 물류 프로세스 표준 조정/정립 필요성(Logistics coordination)
하나의 의약품 혹은 치료약은 유통업체를 통해 수백 개의 병원에 유통되어 각 구매자의 요구사항을 추적하고 충족시키기가 어렵다. 새롭게 부상되고 있는 CAR-T 치료법은 병원 간 프로세스 차이가 제품에 어떤 문제가 될 수 있는지를 보여준다. 다른 많은 면역 종양 약과 달리 CAR-T 치료법은 독특한 공급망 형태를 가지고 있다. 이 약의 생산은 암 환자로부터 T 세포를 추출하는 것으로 시작되고, 추출된 세포는 주입 시설로 보내지기 전에 종양을 보다 효과적으로 표적화 할 수 있도록 유전자 조작을받은 제조 시설로 운송됩니다. 운송 중 세포는 극도로 차가워져야 하는데 그렇지 않으면 죽을 수도 있습니다. 일반적인 치료에 실패한 암 환자는 잘 보관된 의약품 운송이 충분히 빨리 일어나지 않거나 다른 사람의 세포가 주어지면 죽을 수도 있습니다. CAR-T 등 제품에 대한 공급 표준 프로세스가 정립되지 않아 어떤 병원은 암 전이가 발생하기 전에 이 제품을 사용을 요청하여 사용해야 하는 암환자에게 재고고갈로 적시납품이 안되는 경우도 발생하고 있다.
3) 규정준수(Compliance)
의약품의 성분을 구성하는 재료의 80%, 완제품의 40%가 해외에서 미국으로 수입됩니다. 그러므로 미국 FDA(Food and Drug Administration)는 외국에서 생산된 의약품이 무균 생산 표준인 Good Manufacturing Practices를 준수했는지 확인해야합니다.
FDA검사관들이 중국, 인도 등 해외 제조업체에게 품질 및 규제를 준수하라는 경고 메시지를 보냈다. 미국은 2023년까지 제품의 추적성을 강화하기 위해 선사와 운송업체는 의약품공급망안전법(Drug Supply Chain Security Act)의 규제를 준수해야만 한다.
4) 콜드체인운송(Cold-chain shipping)
의약품 같은 생물 제제는 열에 민감하며 오염되기 쉽습니다. 이러한 약을 운송 중 차갑게 유지하는 것은 제약 회사와 환자를 연결하는 공급망의 중요한 부분입니다.
또한 CAR-T 치료법이 각 환자에게 맞춤화되어 있기 때문에 콜드 체인 기술은 신원 확인 및 공급사슬을 세부적으로 유지할 수 있는 추적 소프트웨어와 통합해야합니다.
















